Corrosion galvanique
3 participants
Page 1 sur 1
 Corrosion galvanique
Corrosion galvanique
Salut,
Un commentaire de "Gazou" dans la rubrique "Bon Coin" a attiré mon attention sur les phénomènes de corrosion liés à l’usage simultané de matériaux divers… Un truc dont je ne me suis jamais préoccupé dans mes modèles... Réel problème dans la vraie vie, mais doit-on vraiment s’en soucier dans nos modèles réduits ? J'ai donc décidé de rafraîchir mes connaissances sur le sujet.
Phénomène connu sous différents noms : Corrosion électrolytique, corrosion galvanique, incompatibilité galvanique, etc…
• Un bref résumé du problème pour guider ma réflexion :
Un savant italien, Luigi Galvani, médecin & philosophe découvrit tout à fait par hasard que dans certaines circonstances des pattes de grenouilles reliées à des métaux différents se contractaient (la fameuse expérience de dissection!)… Cette découverte conduisit ensuite le physicien Allessandro Volta à inventer la « pile » électrique… Mais l’effet de base garda le nom de "galvanique" en hommage au bon docteur. Alors de quoi s’agit-il ?
Des métaux différents plongés dans un liquide contenant des radicaux libres (appelé electrolyte) échangent des ions, créant un courant électrique. L’un des métaux va s’oxyder et se dissoudre, l’ anode. L’autre métal va recevoir ces ions et former une couche de composition complexe dépendant du type des métaux en présence avec dégagement d’hydrogène. Il se crée une pile électrochimique.
• Pour qu’il y est corrosion galvanique, il faut donc 4 conditions :
- Un electrolyte dans lequel circuleront les ions. Dans notre cas bien sur de l’eau. Il faut qu’il puisse conduire l’électricité ! Ca marchera beaucoup mieux en eau salée qu’en eau douce. Mais attention l’eau vraiment pure est très rare dans la nature et l’acidité naturelle (ph) joue un rôle similaire et complexe.
- Un métal « A » l’anode dit le moins « noble »
- Un métal « C » la cathode dit le plus « noble »
- Et il faut que le courant puisse circuler, donc qu’il y est un contact métal/métal ou continuité électrique entre les deux métaux.
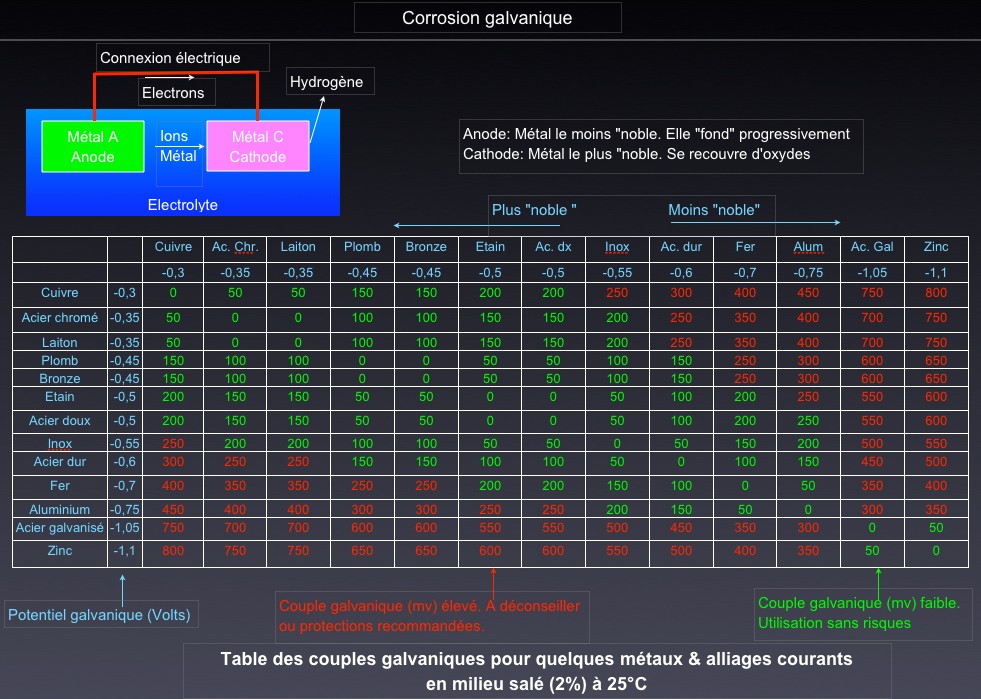
• Les métaux peuvent être classés en fonction de leur « potentiel galvanique ». La différence de potentiel entre deux métaux est appelée « couple galvanique ». Il est alors possible d’établir des tables permettant de prédire les risques de corrosion. Elles sont en général basées sur des mesures réalisées dans de l'eau salée (teneur en sel 2 à 3%), agitée et à 25°C. Plus le couple galvanique entre les deux métaux sera important et plus forte sera la corrosion. Il est admis qu’en dessous de 200mV le phénomène est négligeable.
Tout ça résumé sur la vue ci-dessous.
• Comment traiter le problème ?
Plusieurs méthodes, du plus simple au plus compliqué :
- Choisir des métaux aussi compatibles que possible: Sur une vis en laiton mettre par ordre de préférence un écrou laiton (0mv) ou en inox ( 200mv) plutôt qu’en acier zingué (750mv).
- Couper le circuit électrique en évitant le contact direct des deux métaux, le phénomène s’atténuant très vite avec la distance : Intercaler des rondelles isolantes.
- Eliminer le contact électrolyte/métaux : Très simple avec une couche de graisse (rappelez vous sur vos voitures les plots de batteries en plomb et les cosses en laiton avec une couche de graisse !) . Autre solution très efficace, une bonne couche de peinture (mais faut pas rayer la peinture…)
- Utiliser un troisième métal pour créer une « anode » dite sacrificielle ; c’est elle qui disparaîtra, protégeant les autres métaux. On utilise en général le zinc, l’un des métaux les moins « nobles ».
- Installer un dispositif complexe de contre-accus annulant les courants de corrosion.
• Et sur nos modèles ?
Naviguant principalement en eau douce, le problème est largement atténué et on peut oublier anode sacrificielle et système d’accus !
- Les coques sont généralement en bois donc pas de soucis.
- Les parties métalliques immergés se résument le plus souvent à l’hélice, l’arbre d’hélice, le tube d’étambot & éventuellement le gouvernail et son axe et tube de jaumière.
Un tube de jaumière et un axe en laiton élimineront tout souci. Si l’axe est en acier (tige filetée) un bon remplissage de graisse devrait suffire. Si le gouvernail est métallique, il est préférable de le tailler dans une tôle en laiton monté sur un axe laiton. Sinon le peindre !
Restent les hélices généralement en laiton/bronze sur des axes en acier. Normalement l’axe ne devrait pas être exposé à l’eau et au pire sera couvert de graisse. Donc là non plus pas trop de souci.
Et enfin, nos modèles ne passent pas des mois dans l’eau et sont le plus souvent soigneusement essuyés dès la sortie…
En résumé, avec un minimum de précautions et sauf cas vraiment particulier (coque métallique ou doublée métal) il me semble que la corrosion galvanique ne devrait pas poser de problèmes au modéliste naval… Bon mieux vaut éviter quand même les associations écrous ou vis galvanisés & laiton par exemple. De même aluminium & laiton sans protection. A noter que sur les installations vapeur les problèmes en particulier des joints et de la chaudière seront un peu plus sérieux. Mais ce n' est pas le sujet.
Perso, je n’ai pas remarqué de problèmes sur mes modèles mais j’ai peu d’heures de navigation. Suis-je un poil négligent...
Et vous, avez-vous rencontré des problèmes de corrosion galvanique ? Prenez-vous des précautions particulières ?
Marcel
Un commentaire de "Gazou" dans la rubrique "Bon Coin" a attiré mon attention sur les phénomènes de corrosion liés à l’usage simultané de matériaux divers… Un truc dont je ne me suis jamais préoccupé dans mes modèles... Réel problème dans la vraie vie, mais doit-on vraiment s’en soucier dans nos modèles réduits ? J'ai donc décidé de rafraîchir mes connaissances sur le sujet.
Phénomène connu sous différents noms : Corrosion électrolytique, corrosion galvanique, incompatibilité galvanique, etc…
• Un bref résumé du problème pour guider ma réflexion :
Un savant italien, Luigi Galvani, médecin & philosophe découvrit tout à fait par hasard que dans certaines circonstances des pattes de grenouilles reliées à des métaux différents se contractaient (la fameuse expérience de dissection!)… Cette découverte conduisit ensuite le physicien Allessandro Volta à inventer la « pile » électrique… Mais l’effet de base garda le nom de "galvanique" en hommage au bon docteur. Alors de quoi s’agit-il ?
Des métaux différents plongés dans un liquide contenant des radicaux libres (appelé electrolyte) échangent des ions, créant un courant électrique. L’un des métaux va s’oxyder et se dissoudre, l’ anode. L’autre métal va recevoir ces ions et former une couche de composition complexe dépendant du type des métaux en présence avec dégagement d’hydrogène. Il se crée une pile électrochimique.
• Pour qu’il y est corrosion galvanique, il faut donc 4 conditions :
- Un electrolyte dans lequel circuleront les ions. Dans notre cas bien sur de l’eau. Il faut qu’il puisse conduire l’électricité ! Ca marchera beaucoup mieux en eau salée qu’en eau douce. Mais attention l’eau vraiment pure est très rare dans la nature et l’acidité naturelle (ph) joue un rôle similaire et complexe.
- Un métal « A » l’anode dit le moins « noble »
- Un métal « C » la cathode dit le plus « noble »
- Et il faut que le courant puisse circuler, donc qu’il y est un contact métal/métal ou continuité électrique entre les deux métaux.
• Les métaux peuvent être classés en fonction de leur « potentiel galvanique ». La différence de potentiel entre deux métaux est appelée « couple galvanique ». Il est alors possible d’établir des tables permettant de prédire les risques de corrosion. Elles sont en général basées sur des mesures réalisées dans de l'eau salée (teneur en sel 2 à 3%), agitée et à 25°C. Plus le couple galvanique entre les deux métaux sera important et plus forte sera la corrosion. Il est admis qu’en dessous de 200mV le phénomène est négligeable.
Tout ça résumé sur la vue ci-dessous.

• Comment traiter le problème ?
Plusieurs méthodes, du plus simple au plus compliqué :
- Choisir des métaux aussi compatibles que possible: Sur une vis en laiton mettre par ordre de préférence un écrou laiton (0mv) ou en inox ( 200mv) plutôt qu’en acier zingué (750mv).
- Couper le circuit électrique en évitant le contact direct des deux métaux, le phénomène s’atténuant très vite avec la distance : Intercaler des rondelles isolantes.
- Eliminer le contact électrolyte/métaux : Très simple avec une couche de graisse (rappelez vous sur vos voitures les plots de batteries en plomb et les cosses en laiton avec une couche de graisse !) . Autre solution très efficace, une bonne couche de peinture (mais faut pas rayer la peinture…)
- Utiliser un troisième métal pour créer une « anode » dite sacrificielle ; c’est elle qui disparaîtra, protégeant les autres métaux. On utilise en général le zinc, l’un des métaux les moins « nobles ».
- Installer un dispositif complexe de contre-accus annulant les courants de corrosion.
• Et sur nos modèles ?
Naviguant principalement en eau douce, le problème est largement atténué et on peut oublier anode sacrificielle et système d’accus !
- Les coques sont généralement en bois donc pas de soucis.
- Les parties métalliques immergés se résument le plus souvent à l’hélice, l’arbre d’hélice, le tube d’étambot & éventuellement le gouvernail et son axe et tube de jaumière.
Un tube de jaumière et un axe en laiton élimineront tout souci. Si l’axe est en acier (tige filetée) un bon remplissage de graisse devrait suffire. Si le gouvernail est métallique, il est préférable de le tailler dans une tôle en laiton monté sur un axe laiton. Sinon le peindre !
Restent les hélices généralement en laiton/bronze sur des axes en acier. Normalement l’axe ne devrait pas être exposé à l’eau et au pire sera couvert de graisse. Donc là non plus pas trop de souci.
Et enfin, nos modèles ne passent pas des mois dans l’eau et sont le plus souvent soigneusement essuyés dès la sortie…
En résumé, avec un minimum de précautions et sauf cas vraiment particulier (coque métallique ou doublée métal) il me semble que la corrosion galvanique ne devrait pas poser de problèmes au modéliste naval… Bon mieux vaut éviter quand même les associations écrous ou vis galvanisés & laiton par exemple. De même aluminium & laiton sans protection. A noter que sur les installations vapeur les problèmes en particulier des joints et de la chaudière seront un peu plus sérieux. Mais ce n' est pas le sujet.
Perso, je n’ai pas remarqué de problèmes sur mes modèles mais j’ai peu d’heures de navigation. Suis-je un poil négligent...
Et vous, avez-vous rencontré des problèmes de corrosion galvanique ? Prenez-vous des précautions particulières ?
Marcel

Dernière édition par rookie78 le Ven 14 Déc 2012 - 18:07, édité 1 fois
_________________
Un seul hêtre vous manque... et tout est peuplier ! (Coluche)
Si vous ne pouvez exceller par le talent, triomphez par l'effort. C'est insulter l'éternité que de tuer le temps!
http://www.tournereau.com/modelisme/Accueil/Accueil.html
 Re: Corrosion galvanique
Re: Corrosion galvanique
Hello Marcel
Y a une vue à voir ????Tout ça résumé sur la vue ci-dessous.
_________________
Albertus, du Pays de Herve, là où le fromage sent bon la vache
 Re: Corrosion galvanique
Re: Corrosion galvanique
albertus a écrit:Hello MarcelY a une vue à voir ????Tout ça résumé sur la vue ci-dessous.
Y en a une maintenant... Milles excuses...
Marcel.
--------------
_________________
Un seul hêtre vous manque... et tout est peuplier ! (Coluche)
Si vous ne pouvez exceller par le talent, triomphez par l'effort. C'est insulter l'éternité que de tuer le temps!
http://www.tournereau.com/modelisme/Accueil/Accueil.html
 Re: Corrosion galvanique
Re: Corrosion galvanique
:( Bonsoir!
Merci Rookie!
Voilà une bonne & claire explication qui va permettre de choisir les bons métaux ou pour le moins d'éviter les mauvais.
A consulter sans modération!
Bien cordialment!
Merci Rookie!

Voilà une bonne & claire explication qui va permettre de choisir les bons métaux ou pour le moins d'éviter les mauvais.
A consulter sans modération!
Bien cordialment!

Invité- Invité
 Re: Corrosion galvanique
Re: Corrosion galvanique
Bonsoir,
Merci pour cette explication. Les anodes sont plus nombreuses près des hélices et safrans. Elles sont systématiquement changées lors des dry dock (environ tous les deux ans). Plus de 50% de métal a été bouffé.
Ray 35
Merci pour cette explication. Les anodes sont plus nombreuses près des hélices et safrans. Elles sont systématiquement changées lors des dry dock (environ tous les deux ans). Plus de 50% de métal a été bouffé.
Ray 35

ray 35
 Re: Corrosion galvanique
Re: Corrosion galvanique
Bonsoir! :(
Et bien , nous aurons deux tableaux! On ne devrait plus avoir de problème de corrosion, :mon dieu
On ne devrait plus avoir de problème de corrosion, :mon dieu
Cordialement!

Et bien , nous aurons deux tableaux!
 On ne devrait plus avoir de problème de corrosion, :mon dieu
On ne devrait plus avoir de problème de corrosion, :mon dieu Cordialement!


Invité- Invité
 Re: Corrosion galvanique
Re: Corrosion galvanique
KBIO a écrit:Bonsoir! :(
Et bien , nous aurons deux tableaux!On ne devrait plus avoir de problème de corrosion, :mon dieu
Cordialement!

Salut,
Il existe bien d'autres tableaux! J'en ai bien trouvé une bonne douzaine sur le Net (et je me suis arrêté là...), donnant les couples galvaniques pour non seulement beaucoup de métaux mais aussi d'alliage variés et divers.
J'ai noté aussi que les valeurs données varient un peu d'un tableau à l'autre... Sans doute des conditions de tests légèrement différentes... Ou des alliages pas tout à fait les mêmes: Il existe des tas de variétés de "laiton", "bronze" ou "aciers"... Ou des métaux pas pris dans les mêmes conditions, par exemple Inox passifié ou non...
J'avais donc simplifié tout ça en prenant des "moyennes" pour les trucs courants que l'on utilise sans trop chercher les détails... Mais c'est sur, le tableau de "Graine au vent" est plus technique!!

Au final (heureusement!), on retrouve bien les mêmes associations de métaux à éviter.
 , Marcel.
, Marcel.------------------------
_________________
Un seul hêtre vous manque... et tout est peuplier ! (Coluche)
Si vous ne pouvez exceller par le talent, triomphez par l'effort. C'est insulter l'éternité que de tuer le temps!
http://www.tournereau.com/modelisme/Accueil/Accueil.html
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|

